�sȩ���Ͼ��ǵ��Ƃ估����푑���
�r�g��2020��03��26�� ����r�IՓ�� �Δ���
����ժҪ��ͨ�^�sȩ�I�������������������h�������嶡������ˮ���F�քe���뵽�Ͼ�������ϣ��Ƃ���һϵ���������Կsȩ���Ͼ��ǡ�ͨ�^�˴ŷ���������-��Ҋ���V�yԇ�˿sȩ���Ͼ��ǵĽY������푑��ԡ��Y���������ƵõĿsȩ���Ͼ��Ǿ�����ͬ�u��ȡ���ȣ���ȫ����ǭh��sȩ�Y��������푑����c�sȩβλ��̼ԭ�����P������������Ͼ�����Ҫ���͵�pH����ˮ�⣬�嶡������Ͼ��Ǿ��и��`������푑��ԡ�
�����P�I�~���Ͼ���;�sȩ;��푑���
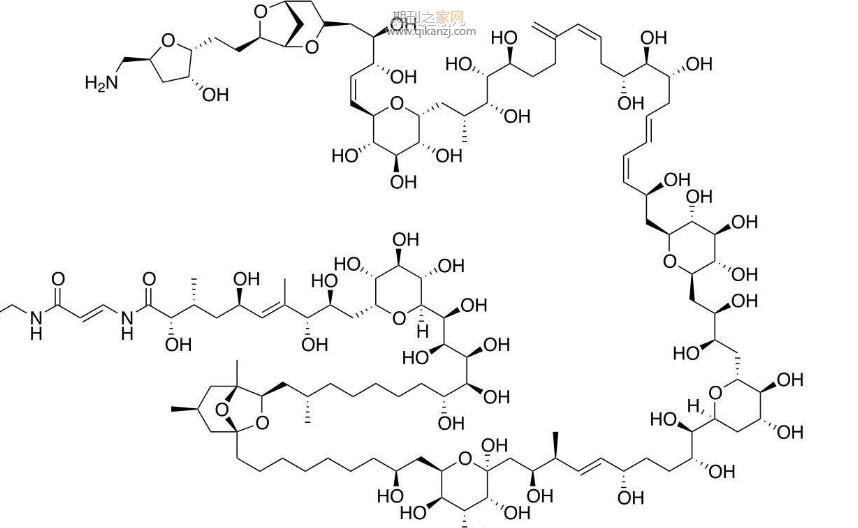
�����sȩ���ЙC�ϳ��б��V�������u���ı��o���F�������ԗl���¿���Ó���o[1]����������푑���[2]��һϵ�к��пsȩ�I�IJ��ϱ�������푑��Բ���[3,4]���sȩ���Ͼ�������ˮ�Ŀsȩ���Fȡ���Ͼ������Hˮ���u���Ƃ����[5]�������Ƃ�l���غͣ���ֻ����ˮ�г������ɼ�������������V�������ڴ̼�푑�ˎ���f���I��[6,7]��Broaders��[6]���sȩ�����Ͼ������������ί���ˎ���d�w��Cohen��[7]���sȩ�����Ͼ������ڂ�ݔС�ɔ_���Ǻ���(siRNA)���c���ұ�����(PLGA)������ɽ�����ϲ�ͬ[8]���sȩ�����Ͼ��Ǵ��x�a��]�ж�������[9]�������p���ֲ��M��[10]��
�����P�ڽY�����sȩ���Ͼ�����푑��Ե�Ӱ�����һЩ���[11]�����������ш���īI���ü�������ϩ����������ϩ�����|������Ͼ��ǣ��Ƃ�Įa���u��ȡ�����y�Կ��ƣ��ҭh��sȩ�Y���;��Կsȩ�Y������[12]������ͬ�u��ȡ�����£��h��;��Կsȩ��ռ������ͬ�����ϵ���푑���Ҳ��Ӱ�[13]����ˌ��ڿsȩ�����Ͼ��ǵ���푑���Ӱ��������д������о���
���������Mһ���о�Ӱ푿sȩˮ�����ʵ����أ�����ʹ����ϩ��������|(��������ϩ���ѡ���������ϩ���ѡ��嶡����ϩ���ѡ��h������ϩ����)�Ƃ���һϵ�и����Ͼ��ǡ��˴ź����~׃�Q�t����V�C���Ƃ�õ���Ŀ�ˮa��ú˴ŷ����˿sȩ���Ͼ��ǵ�ˮ��a�����������C���Ƃ�õ��˾��������u��ȡ���ȵĿsȩ���Ͼ��ǣ������γɷǭh��sȩ�Y�����Mһ���γɭh��Y�����]��С����Ó�����_���܉�����ͬ�ėl�����о��sȩ��ˮ�⡣�о��Y���������sȩβλ��̼ԭ����͌��sȩ����푑����ЛQ����Ӱ푣�����ͬpH�l���£��Ƃ�Ŀsȩ���Ͼ�����βλ����̼�Ŀsȩ���Fˮ��������죬��βλ�鲮̼�Ŀsȩ���Fˮ������������
����1����
����1.1ԭ�Ϻ�ԇ��
�����Ͼ���(Mw=4×104)���tˎ�����Ϻ������������Ƽ�����˾��ʹ��ǰ�����ɳ�ˮ̎��;��������ϩ���ѡ���������ϩ���ѡ��h������ϩ���ѡ���������������}�����������_�����W���g(�Ϻ�)����˾;�嶡����ϩ���ѣ������������ϣ��˼�����Ƽ�����˾;��������(DMSO)�������������_��˹���Wԇ������˾��ʹ��ǰ��0.4nm���ӺY����̎��;������(w=98%)�����Ұ����״�����80������������ˎԇ������˾;뮴��}�ᡢ뮴�DMSO����ˮ�����u�v����˾��
����1.2��Ʒ�Ƃ�
����1.2.1�oˮ�Ͼ��ǵ��Ƃ�
�������ڿsȩ���������ˮ�ֵ�Ӱ푣��ڌ��ǰ�����Ͼ����M�г�ˮ̎����������ڳ�����£���늟��L���M�мӟᣬ��ȥ�����ˮ�֣�������Ԛ��w���������Ȼ��s�����M�мӟ����ճ�ˮ������3�Ρ�����м���10.0g�Ͼ��ǣ���Q��3�Σ��ټ���150mL�oˮDMSO����������ȫ�ܽ⣬����0.4nm���ӺY������48h���á�
����1.2.2�sȩ���Ͼ��ǵ��Ƃ�
�������ȣ�������M�мӟ����ճ�ˮ����3��;�������댦�ױ���������}20.0mg����Q��3��;Ȼ������Ͼ��ǵ�DMSO��Һ15mL(����1.00g�Ͼ��ǡ�16.6mmol�u��)�����������ױ���������}����������ȫ�ܽ��քe������ϩ��������834mg(8.3mmol)����ϩ��������834mg(8.3mmol)���h������ϩ����1.05g(8.3mmol)���嶡����ϩ����834mg(8.3mmol)���Ҝؔ���12h;�����1.0mL���Ұ���練����������Һ�μ��볬��ˮ�г������x��(8000r/min��5min)�ռ����w���ٌ����w�ܽ��ڼ״��У��ڳ���ˮ�г������x��(8000r/min��5min)�ռ����w�������w���ɺ���ã������ĮaƷ�քe������������Ͼ��ǡ�����������Ͼ��ǡ��h��������Ͼ��ǡ��嶡������Ͼ��ǡ�
����1.2.3�sȩ���Ͼ��Ǒҝ�Һ���Ƃ�
��������pH�քe��1��2��3��4��5��������Һ(����w=1%����80)���քeȡ10.0mg�����Ͼ��ǘ�Ʒ�ܽ���1.0mL�״��У������μ��벻ͬpH��������Һ�У��Ƃ�õ������Ͼ��ǵđҝ�Һ���ڲ�ͬ�r�g�c�y����ȡ�
����1.2.4�sȩ���Ͼ��ǵ�ˮ��
�����քeȡ5.0mg�����Ͼ��ǘ�Ʒ���ܽ���0.5mL뮴�DMSO�У�����0.1mL뮴��}�ᣬ������ں˴Ź��У��ʂ�˴ű�����
����1.3�yԇ�c����
����ʹ�õ�Bruker��˾AVANCE300�˴Ź����V�x�y���˴Ź�����V;�����~׃�Q�t����V������Bio-Rad��˾Win-IR�t����V�x�y���������廯⛉�Ƭ��;��������V������PerkinElmer��˾Lambda365����-��Ҋ�ֹ���Ӌ�y����
����2�Y���cӑՓ
����2.1�sȩ���Ͼ��ǵı���
�������Wλ��0.84��1.45̎��������CH3CH2CH2�D�������壬���Wλ��0.85̎�鮐�����ϼ��������壬���Wλ��1.20��1.80̎��h�����������壬���Wλ��1.17̎���嶡���������塣�Ͼ��ǺͿsȩ���Ͼ��ǵļt����V���ڿsȩ���Ͼ����У�1650cm−1̎���u������������շ�ď���׃����2874cm−1��2873cm−1��2857cm−1��2937cm−1̎���F�µĨDCH�D���շ塣�˴źͼt��Ĕ����C���ɹ��Ƃ���һϵ�пsȩ���Ͼ��ǡ�
����2.2�sȩ���Ͼ��ǵ�ȡ����
�������ڿsȩ���Ͼ��ǵĺ˴ŷ�o���M�Мʴ_�ķe�ց�Ӌ��ȡ���ȣ����Ԍ�뮴��}����뵽�sȩ���Ͼ��ǵ�뮴�DMSO��Һ�У����sȩ���Ͼ���ˮ���������ˮ��a����M�зe��Ӌ���u��ȡ���ȡ�����ˮ��a����ȩ���c�ͣ��ד]�l������С������Nˮ��a�������M��ȡ����Ӌ�㡣���^Ӌ��ɵã�����������Ͼ��ǡ�����������Ͼ��ǡ��h��������Ͼ��Ǻ��嶡������Ͼ��ǵ�ȡ���ȷքe��49.0%��49.0%��49.9%��50.0%���õ���ȡ���ȷdz��ӽ��Ŀsȩ���Ͼ��ǡ�
�������⣬����Ͷ�ϕr�����u��ȡ����50.0%�M��Ͷ�ϣ����a�����������С������N��ռ�u�������cͶ�ϕrС������N��ռ�u������һ�£���˛]����NС�����Mһ���l���h���sȩ�������Ͼ������Ó�����ʱ��о��Ƃ�Ŀsȩ���Ͼ��Ǿ���ǭh��Y����ȡ���ȷdz��ӽ���
����2.3�sȩ���Ͼ��ǵ���푑���
�����c����������|������a�����Ե����ͬ���sȩ���Ͼ��ǵ�ˮ��a��ȫ�����������|�������Ɖľֲ�����A�ԣ����������pH=2��������Һ�M����푑��yԇ����pH=2��������Һ�У���푑������ɿ쵽�����Ξ��嶡������Ͼ��ǡ��h��������Ͼ��ǡ�����������Ͼ��ǡ�����������Ͼ��ǡ�
����3�YՓ
����(1)���Üغͺ���ķ����Ƃ��˲�ͬ�sȩ���F���Ե��Ͼ��ǡ�
����(2)�Ƃ�Ŀsȩ���Ͼ��Ǿ�����ͬ���u��ȡ���ȣ��Ҟ�ǭh��sȩ�Y����
����(3)��ͬ��ȡ�������sȩ���Ͼ��ǵ���푑��Ծ��в�ͬӰ푣��sȩβλ̼ԭ�ӵ���͛Q���˿sȩ���Ͼ��ǵ���푑��ԣ���푑����ɏ�������������̼ȡ������̼ȡ������̼ȡ����
���������īI��
����CORDDESEH,BULLHG.Mechanismandcatalysisforhydrolysisofacetals,ketals,andorthoesters[J].ChemicalReviews��1974��74(5)��581-603.
����[1]BACHELDEREM,BEAUDETTETT,BROADETSKE,etal.Invitroanalysisofacetalateddextranmicroparticlesasapotentdeliveryplatformforvaccineadjuvants[J].MolecularPharmaceutics��2010��7(3)��826-835.
����[2]BACHELDEREM,BEAUDETTETT,BROADERSKE,etal.Acetal-derivatizeddextran:Anacid-responsivebiodegradablematerialfortherapeuticapplications[J].JournaloftheAmericanChemicalSociety��2008��130(32)��10494-10495.
SCI�ڿ�Ŀ�
���T�����ڿ�Ŀ�
SCIՓ��
- 2023-07-06��ʿ��SSCI�ڿ��l��Փ�Ľ��v��Ҫ
- 2022-11-10ssci��Ͷ�嵽�l��Ҫ���?
- 2024-04-01ANNALS OF PHYSIC���·օ^�ǎׅ^
SSCIՓ��
- 2023-06-14�lssciՓ���ܲ鵽���ԃ����
- 2023-12-25AHCI�l��Փ����W�g�ɹ���
- 2023-08-24Փ�İl����ÿ��Ա�ssci���
EIՓ��
- 2022-12-07ei�ڿ�Փ�İl�����y�Ȇ�
- 2023-06-28ieee xplore ��ei�z����
- 2023-02-07ei���h��ǰ����_ʼ����
SCOPUS
- 2023-03-28scopus�����Щ�W�Ƶ��ڿ�
- 2023-03-20scopus���z���������
- 2023-04-12scopus�����������Щ�T��īI
���g��ɫ
- 2023-05-09������P����������ô���g��Ӣ��
- 2023-05-11�����t�WsciՓ�ĝ�ɫ���Æ�
- 2023-05-06����y��������ô���g��ɫ
�ڿ�֪�R
- 2020-08-05sciՓ����ô��
- 2022-04-02Փ��������l��Ҫ��������
- 2015-06-05�l���ڽ�����µĺ����ڿ�
�l��ָ��
- 2020-07-28�R������Փ�İl���x������
- 2018-03-17��������������ڿ���ÿ���
- 2022-03-15����ͯ�����Ѱl���^��Փ��