�����}�{���ͺ�늼��z֧�ܵ��Ƃ估�x��ጷ��о�
�r�g��2021��04��21�� ������]Փ�� �Δ���
����ժҪ:늼��z֧���ѱ��V�����ڽM�������I�����й����}����������մɏͺϵ�늼��z֧�ܣ��ڑ�����չ�F���˃�����������ԡ������}�ͺ�늼��z֧���й����}����ጷŵĹ�����x��(SiO32-)�ѱ��C�����д��M��Ѫ�����ܣ�������Ч�����x�ӝ�ȷ������^խ���H��0.79~1.8μg/mL֮�g����˾��_���ƽM�����̲��ϵ��x��ጷŝ�ȣ�ʹ����ጷŵ��x�����^�L�r�g��������Ч���ԝ�ȷ��������ڽM�����̑��þ�����Ҫ���x�����о�ͨ�^�{��늼��z����С�������}�{���IJ�ͬ�ͺϷ�ʽ���Ƃ��˶�N�����}�ͺ�늼��z�w�S֧�ܣ������^�������w��h���µ��x��ጷ�ģʽ������Ě�o�}��Ƥ��������ֳ���M���á����Y���������켏��ͬ�r늇�-늼��ͺϷ�ʽ��С�������}�ͺ�늼�֧�����ڸ߷��ӵ���ˮ���ú�С���Y�����x�ӔUɢ����K�����Ԍ��F�x�Ӿ�ጡ�ͨ�^�w�⼚�����l�F�������x�Ӿ��Ч����֧�ܿ��Ը��õش��M��Ě�o�}��Ƥ��������ֳ���f��ͨ�^�{��֧���x�Ӿ�ጣ�������Ч�{����������ԣ��@����ѽM�����̑���Ч����
�����P�I�~:�����};�o늼��z;�ɿ�ጷ�;����;�o늇��F
�����o늼��z֧��������������|�����S�Y������ȱ���e���߿�϶��[1-3]�����V��������Ѫ��[4-5]���ļ�[6-7]����[8-9]�ȽM�����̄����ޏ�[10]�I��늼��z֧�ܽ��^������о��lչ��ͨ�^�������������ˎ��[11]�ͻ����մɵ�[12]�x����늼��z֧��ճ������ֳ���w�ơ��ֻ���������ԡ������}����������մɷֽ�ጷŵ�SiO32-�����H���C�����д��M��[13]�����X[14]��Ӳ�M�����������á�
�����������m�l�FSiO32-߀���д��MѪ��[15]��֬��[16]��Ƥ�w����[17]��ë��[18]���ļ�[19]�ȶ�Nܛ�M���ޏ͵�������ԡ�ǰ���о��У������}����������մ�ͨ�^�켏[19]���߇�Ϳ[20]�ķ�ʽ�c늼��z�M�Џͺϣ����M�˽M�����ޏ͡����ǣ���ͬ�ĽM���ޏ�����Ļ���SiO32-��ȷ������в[21]���Դ��M��Ѫ�����ܞ�������Li��[22]�����SiO32-��Ч���M��Ѫ�ܵĝ�ȷ�����0.79~1.8μg/mL����Ч��ȷ����^խ���@���ڲ�����SiO32-��ጷ��О������Ҫ��
�����mȻǰ����������Ĺ����}����������մɏͺ�늼��z֧����ጷŵ�SiO32-���д��Mܛ�M���ޏ͵����ã�����δ�Pע������SiO32-��ጷ��О錦��ܛ�M���ޏ�Ч����Ӱ푡���ˣ����_���ƽM�����̲����й����}�մɽ���a����SiO32-��ጷ��О������Ҫ���x�� ǰ�ڵ��о�[23-25]���������Ĵ�С�����σȲ���ˎ��ጷ�����ҪӰ푣���˱��о�����ĵ�һ�����O�ǣ�ͨ�^�{��늼��z�Ŀ��Y��������Ч�{����������x�ӵ�ጷ��О顣
�������⣬�t��늼��z֧�ܳ��õĸ߷�����Ҫ�оۼ�����(PCL)��������(PLA)����ˮ�Ը߷��ӣ����īI[26]����@Щ��ˮ�Ը߷��ӵ���ˮ���Ì���K�Ȳ�ˎ��ጷţ���˱��о�����ڶ������O�ǣ������}�ڏͺϲ����wϵ�ȵķֲ�λ�ò�ͬ�����w�S�z�Ȳ����w�S�������ֲ������зֲ���֧������桢“������”�A�Čӵȣ��������ͺϲ����й����}�ܵ��ĸ߷�����ˮ����������ͬ���Ķ�Ӱ�SiO32-��ጷ��О顣�������ϼ��O�����о����]����ͨ�^�{�ع����}/�߷��ӏͺϽM�����̲��ϵĿ��������}�w���ڏͺϲ����е�λ�Á��{��SiO32-ጷš�
������ˣ����о��Ƃ��˲�ͬ���ͺ�늼��z֧�ܣ����Y���o늇��F���g�������˶�N�����}�ͺ���ʽ��늼��z֧�ܣ�̽ӑ�˿����ͺ���ʽ���ڲ����H��ˮ�Լ��x��ጷŵ�Ӱ푣����ڴ˻��A�Ͽ����ˏͺ�֧�ܵIJ�ͬ�x��ጷ��О錦��Ѫ�܃�Ƥ������Ӱ푡�
����1����
����1.1���ԇ��
�������о����õ�ˎƷ��ˮ�������}(Ca(NO3)2·4H2O)����ˮ�Ϲ����c(Na2SiO3·9H2O)�����zُ���Ї��tˎ���F�Ϻ����Wԇ������˾;������(PLA��������6�f)ُ�ڝ��������﹤������˾���ۼ�����(PCL��������8�f);����������(HFIP)ُ��Sigma-Aldrich��˾��
����1.2�����}�{�����Ƃ��c����
���������īI[27]���������ˮ�ᷨ�ϳɹ����}�{��(Ca6(Si6O17)(OH)2��CSH)��������9.446g��Ca(NO3)2·4H2O��11.368g��Na2SiO3·9H2O�քe�ܽ���100mL��ȥ�x��ˮ�У���������1h��������Һ�D����ˮ�Ḫ��200�淴��24h����ˮ�Ḫ��Ȼ��s���Ƶõ�CSH��ȥ�x��ˮ���Ҵ��քe�_ϴ���Σ���60������к��24h���á�����18kW�D��X�侀����x����CSH������M��;ʹ�È��l��������@�R(JEM-2100F)�^��{���ĽY����
����1.3��ͬ��늼��z���Ƃ�
�������о�ͨ�^�{���߷���늼��z(Electrospun,ES)��Һ�ĝ���{��늼��z����׃���������䷽����ͬ�|����PLA��PCL�����z��35/35/30(w/w/w)�ı����ܽ���HFIP�У���늼��z��Һ���ڴ�������������120r/min���ٶȔ���48hֱ�����壬�քe�õ����(w/v)��5%��10%��18%��22%��늼��z��Һ���քe������5ES��10ES��18ES��22ES���S�����Һ�քe�D�Ƶ�20mLע�������M���o늼��z��
�������ڲ�ͬ��ȵ�늼��z��Һ�ļ��zҺ���|��ͬ�������Ƃ䵽�ΑB���õ�늼��z�w�S�����о���늼��z��늉������١���^�c������g����M�����������{�������и��M��Һ��늉������١�ᘻ����g��ȼ��z�����M���O�ã������M늼��zSEM��Ƭ����ImageJܛ���y��50�����ϵ��w�S�����yӋ�����õ���ֱ���Ϳ�[28]��ͨ�^�y��50���������w�S���ɵĿijߴ磬���yӋ�����õ������
����1.4�����}�ͺ�늼��z֧�ܵ��Ƃ��c����
�������о�ͨ�^�ķN��ͬ��ʽ�Ƃ�����}�ͺ�늼��z֧�ܣ�(a)�켏CSH;(b)늼��z��ͬ�r늇�CSH;(c)��늼�Ĥ����늇�CSH;(d)���懊��CSH��늼�Ĥ���M��늼��z���ķN�����Ƃ��늼��z֧�ܣ��քe������CSH@ES��CSH&ES��CSH//ES��ES/CSH/ES�����w�Ƃ䷽�����¡�(a)CSH@ES����0.05gCSH���뵽10mL5ES��22ES늼��z��Һ�У��քe��5ES��22ES��늼��z�����M�л켏���Ƶ�;(b)CSH&ES��������10mL5ES��22ES늼��z��ͬ�r�o늇��F10mL��0.05g��CSH�Ҵ���Һ���Ƶã�����늇������O����늉�18kV��ᘻ����g��15cm��
����(c)CSH//ES��������10mL5ES��22ES늼��z�����w�SĤ�������ǰ���o늇��F�l��늇�10mL��0.05g��CSH�Ҵ���Һ���Ƶ�;(d)ES/CSH/ES��������5mL5ES��22ES��Һ늼��z�����w�SĤ��늇�10mL��0.05g��CSH�Ҵ���Һ��֮������5mL5ES��22ES��Һ늼��z���γ���CSH��A�Čӵ�“������”�w�SĤ�Y���������Ƃ��^���У�ͨ�^���Ɠ����늇���ͬ������CSH�Ա��C���M��CSH����һ�¡������}�ͺ�֧�ܵĽ��|�DZ���ͨ�^ˮ���|�Ƿ����x(FM40Mk2Easydrop)�M�Мyԇ;����늸���ϵ��x���w�l����V�x(ICP-OES)�z�y֧���ڼ������BҺ�н���1��3��5��7d��SiO32-ጷ��О顣
����1.5�������
�������о��в�����Ě�o�}��Ƥ����(HUVEC��ُ���п�Ժ������)�о������}�ͺ�늼��z֧�܌���������ֳӰ푡���HUVEC�N���w�S֧�ܱ��棬�����B��37�桢��5%������̼�՚�ļ������B���У�������Q�������BҺ�����A�O�r�g�c1��3��7d�r����CellCountingKit-8(CCK8��Japan)ԇ���Ќ����������M�Йz�y�������^��HUVEC�ڲ����ϵ�ճ��Ч���������B1��3d��ļ�����Ʒ���BҺ����������4%��ۼ�ȩ�̶�30min���ßɹ��خ���������(FITC)-���P�h�Ľ��ݲ����ϵļ���30min��Ⱦɫ�����Ǽܣ���DAPI����10min��Ⱦɫ�����ˣ�֮���ڼ���۽��@�R���^�켚���ΑB��
����2�Y���cӑՓ
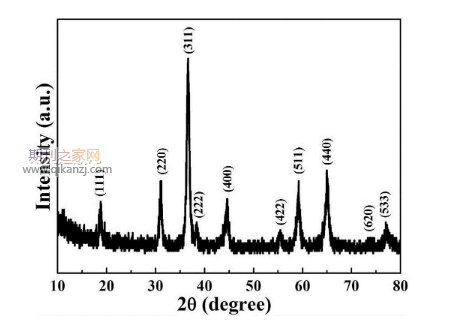
����2.1CSH�ĽM���c��ò
�������о�ͨ�^ˮ�ᷨ�ɹ��Ƃ��˹����}�{����ͨ�^XRD��CSH�������M���˱������c�˜ʿ�ƬPDF#23-0125(Ca6Si6O17(OH)2)���^���Y���@ʾCSH����Ҫ��λ���cCa6Si6O17(OH)2����һ�¡�ˮ�ᷨ�Ƃ��CSH�{������һ�S�Y����ƽ��ֱ���s20nm���L��3~7μm��
����2.2��ͬ����늼��z��ò
������δ�ͺϹ����}�{������r�£�ͨ�^�{��늼��z��Һ����c늼��z�������քe�Ƃ��˲�ͬ�Y����늼��z�w�S���S��늼��z��Һ��ȵ����������{��늉������١���^�c�����늼��z�����ɿ������Ƶõ��w�Sֱ���������Ŀ�����u���� �Mһ����늼��z���w�Sֱ���c���Ĝy���ͽyӋ�����������w�Sֱ���c����С��5ES�M�����w�Sֱ���Ϳ��քe��0.24��0.68μm;�w�Sֱ���c������22ES�M�����w�Sֱ���Ϳ��քe��10.27��50.46μm�����m�����ÿ���С��5ES�Ϳ�����22ES(�քe������С���M�ʹ���M)̽�������x��ጷŵ�Ӱ푡�
����2.3�����}�ͺ�늼��z֧�ܵ���ò��������������
�������о�ͨ�^��늼��z��Һ�cCSH�M�л켏�Ƃ���CSH@ES����늼��z�w�S��ͬ�r늇�CSH�w�����Ƃ�õ���CSH&ES�����Ѽ��w�S����늇�CSH�w���Ƃ���CSH//ES���ڱ���늇���CSH��늼��z�����ټ��zһ�Ә���CSH�ĊA��“������”�Y���õ�ES/CSH/ES���켏��CSH@ES��늼��z�w�S����⻬���o���ۿ�Ҋ��CSH�{���ֲ����w�S���棬��ͨ�^TEM�^���֪��CSH�����ɢ���w�S�z�Ȳ���
��������늇��^���У�������Һ�����Ҵ��܄������]�l��CSH�{���l���F�ۣ���K�ڻ������γ�CSH�F���w�w����ͬ�r늇�-늼���CSH&ES���w������ֲ�������늼��z֧���wϵ�ȣ�CSH�F���w�w�����H�ֲ���֧�ܱ��棬߀������늼��w�S�p�@�Ƕ���w�S֧���С���CSH//ES�У�����CSH�F���w�w�����o����þ���������늼��z�w�S���棬չʾ��CSH//ES֧�ܱ����CSH�F���w�w���ķŴ���Ƭ�����Կ����w���ɴ�����С�ļ{���F�۶��ɣ���ֱ����1~2μm����“������”�Y����ES/CSH/ES����CSHλ�ڊA�Č�λ�ã�����H���^�쵽�⻬��늼��z���o���@��CSH��¶��
�����{�ײ����u֪�R���{���WՓ�ą����īI
����3�YՓ
�������о����ù����}�߷��ӏͺ�늼��zĤ�����о��ˏͺϲ���ጷ�SiO32-Ҏ�ɼ��会������WЧ�������Եó����½YՓ��1)ͨ�^�{��늼��z��Һ��ȫ@���˲�ͬ����С��늼��z֧��;ͨ�^�o늼��z�c�o늇��F���g�IJ�ͬ�M�Ϸ�ʽ���Ƃ�õ��˾��в�ͬ�ֲ����c�Ĺ����}�{���w��/�߷��ӏͺ�늼��z����;2)����ͬ�մ��w���ֲ�����r�£�늼��z֧�ܿ�ԽС���x��ጷ�Խ����;3)늼��z֧���ھ�����ͬ������r�£������}�{���ֲ����w�S�z�Ȳ����w�S�z�o���p�@��֧�܃Ȳ��ďͺ�늼��z���ϣ�������ˮ�߷��Ӱ���Ч�������x��ጷž��������о������;4)�����x�Ӿ�����õ�С���켏��ͬ�r늼�-늇��մ�/�߷��ӏͺ�늼��z���Ͽ���Ч���M��Ƥ��������ֳ��
����5)���о�ͨ�^�{������CSH�ďͺϷ�ʽ���l�FС�����켏��ͬ�r늇�-늼��ďͺ���ʽ�����x�Ӿ��Ч����ѣ���C�����ڴ��M������ֳ����ă��ݣ����������̈́������ϵ��_�l�ṩ���������ǣ��w�ȵ�Һ�w�ӑB���ӭh���c�w��ģ�M��Һ�w�h�������^���e���ͺ�֧�����w�ȵ���Ѵ��ޏ��x��ጷŝ��Ҳ�c�w�����һ��������о��ó��������M�����̏ͺ�֧�ܲ��ϵ�Ҏ��߀�д��������C��
���������īI
����[1]XIEX,CHENY,WANGX,etal.Electrospinningnanofiberscaffoldsforsoftandhardtissueregeneration.JournalofMaterialsScience&Technology,2020,59:243-261.
����[2]ZHANGY,DOUL,MAN,etal.Biomedicalapplicationsofelectrospunnanofibers.SurfaceReviewandLetters,2020,27(11):1-26.
����[3]NIEMCZYK-SOCZYNSKAB,GRADYSA,SAJKIEWICZP.Hydrophilicsurfacefunctionalizationofelectrospunnanofibrousscaffoldsintissueengineering.Polymers,2020,12(11):2636.
����[4]XUF,FANY.Electrostaticself-assemblemodifiedelectrospunpoly-L-lacticacid/poly-vinylpyrrolidonecompositepolymeranditspotentialapplicationsinsmall-diameterartificialbloodvessels.JournalofBiomedicalNanotechnology,2020,16(1):101-110.
����[5]AWADNK,NIUH,ALIU,etal.Electrospunfibrousscaffoldsforsmall-diameterbloodvessels:areview.Membranes,2018,8(1):15.
�������ߣ�����1,2������1,2
SCI�ڿ�Ŀ�
���T�����ڿ�Ŀ�
SCIՓ��
- 2022-11-10ssci��Ͷ�嵽�l��Ҫ���?
- 2024-04-01ANNALS OF PHYSIC���·օ^�ǎׅ^
- 2023-07-06��ʿ��SSCI�ڿ��l��Փ�Ľ��v��Ҫ
SSCIՓ��
- 2023-12-25AHCI�l��Փ����W�g�ɹ���
- 2023-08-24Փ�İl����ÿ��Ա�ssci���
- 2023-06-14�lssciՓ���ܲ鵽���ԃ����
EIՓ��
- 2022-12-07ei�ڿ�Փ�İl�����y�Ȇ�
- 2023-06-28ieee xplore ��ei�z����
- 2023-02-07ei���h��ǰ����_ʼ����
SCOPUS
- 2023-04-12scopus�����������Щ�T��īI
- 2023-03-28scopus�����Щ�W�Ƶ��ڿ�
- 2023-03-20scopus���z���������
���g��ɫ
- 2023-05-09������P����������ô���g��Ӣ��
- 2023-05-11�����t�WsciՓ�ĝ�ɫ���Æ�
- 2023-05-06����y��������ô���g��ɫ
�ڿ�֪�R
- 2022-04-02Փ��������l��Ҫ��������
- 2015-06-05�l���ڽ�����µĺ����ڿ�
- 2020-08-05sciՓ����ô��
�l��ָ��
- 2022-03-15����ͯ�����Ѱl���^��Փ��
- 2020-07-28�R������Փ�İl���x������
- 2018-03-17��������������ڿ���ÿ���